Zasady działania algorytmu oceny suplementów diety z maślanem sodu
Nasz algorytm ocenia skład każdego produktu, łącznie przyznając od 0 do 100 punktów. Z algorytmu korzystamy w rankingu:
RANKING SUPLEMENTÓW DIETY Z MAŚLANEM SODU
Algorytm maślanu sodu Wybieramy Kolagen ocenia (kliknij, by przejść do sekcji):
Co ocenia algorytm maślanu sodu? Za co daje najwyższe oceny?
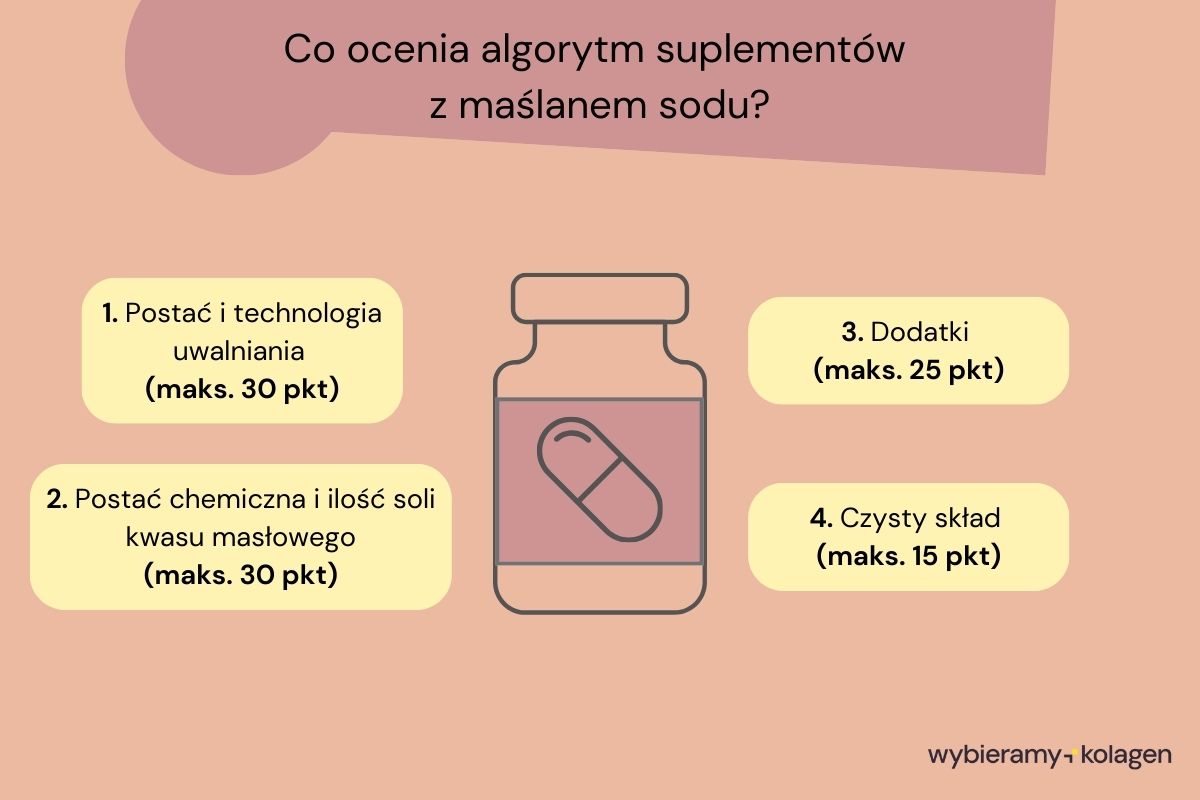
Suplementy diety z maślanem sodu mogą otrzymać najwięcej punktów w 4 kluczowych kategoriach.
- Maks. 30 pkt za postać chemiczną, ilość czystego kwasu masłowego i jego soli – różne sole maślanu zawierają różny procent czystego kwasu masłowego, co oznacza, że ta sama porcja mg rożnych soli może dostarczać zupełnie inną ilość substancji aktywnej. Rodzaj soli, jej porcja oraz rzeczywista ilość kwasu masłowego pokazują, ile aktywnej substancji faktycznie dostaje organizm.
- Maks. 30 pkt za postać i technologię uwalniania – ponieważ to właśnie one decydują o realnej wartości biologicznej suplementu, czyli w którym odcinku układu pokarmowego kwas masłowy się wchłonie. Kluczowe jest, aby dotarł do końcowego odcinka jelia grubego [1-20].
- Maks. 25 pkt za dodatki funkcjonalne – oceniamy probiotyki, prebiotyki i synbiotyki, a także witaminę D czy składniki metaboliczne. Jeśli producent dobiera je właściwie, mogą zwiększać efekty suplementu, poprawiać komfort jelitowy i wspierać cały mikrobiom [8-12].
- Maks. 15 pkt za czysty skład – pomimo różnic w formie suplementu i związanych z tym wymogów technologicznych nie wszystkie dodatki są konieczne. Dobrze skomponowany suplement z maślanem sodu nie potrzebuje dodatkowych konserwantów, sztucznych barwników i innych, zbędnych dodatków technologicznych [4-5].
Skuteczność suplementu z maślanem sodu zależy od czegoś więcej niż tylko „mg na opakowaniu”. Aby realnie ocenić wartość preparatu, trzeba uwzględnić jego formę technologiczną, postać chemiczną, ilość aktywnej substancji oraz obecność składników, które wspierają właściwości maślanu. Każdy z tych elementów wpływa na to, ile kwasu masłowego faktycznie dotrze do jelita grubego, czyli miejsca, w którym działa.
Opracowaliśmy wielopoziomowy model oceny, który pozwala rzetelnie porównywać suplementy między sobą i oddzielić produkty dobrze zaprojektowane od tych, które bazują wyłącznie na marketingu.
Poniżej przedstawiamy szczegółowe kryteria, jak nasz algorytm ocenia suplementy z maślanem sodu.
Postać chemiczna, ilość czystego kwasu masłowego (maks. 30 pkt)
Podobnie jak w przypadku innych suplementów, forma chemiczna maślanów ma znaczenie. Różne sole kwasu masłowego – maślan sodu, potasu, wapnia różnią się między sobą nie tylko zawartością czystego kwasu masłowego (BA), ale również rozpuszczalnością i profilem działania [1-9].
Najlepiej przebadaną formą jest maślan sodu, co potwierdzają liczne przeglądy [1-9]. Dlatego za maślan sodu przyznajemy najwięcej punktów.
Różnice między solami nie są wyłącznie teoretyczne – mają praktyczne znaczenie metaboliczne. W badaniu z 2025 roku naukowcy wykazali, że różne formy maślanów mają odmienne efekty metaboliczne i zapalne [1-9].
W suplementach producenci najczęściej podają ilość soli maślanu (np. maślan sodu 600–720 mg), ale faktyczną substancją biologicznie aktywną jest kwas masłowy (butyric acid, BA). Każda sól maślanu ma inną zawartość czystego kwasu masłowego:
- maślan sodu – ok. 80% kwasu masłowego,
- maślan potasu – ok. 70% kwasu masłowego,
- maślan wapnia – ok. 82% kwasu masłowego.
Suplement, który zawiera „600 mg maślanu sodu” faktycznie dostarcza jedynie około 480 mg czystego kwasu masłowego.
Gdy oceniamy czysty kwas masłowy, możemy porównywać produkty realnie, niezależnie od użytej soli czy zabiegów marketingowych.
To kluczowe, bo to właśnie kwas masłowy metabolizują enterocyty (komórki, które budują nabłonek kosmków jelitowych) i działa biologiczne, m.in. przeciwzapalnie, regeneracyjnie, metabolicznie i barierowo.
Część producentów stosuje mieszanki soli soli kwasu masłowego, np. maślanu sodu z maślanem wapnia. Nie ma jednak dowodów naukowych, że takie połączenia zwiększają efekty suplementu. Często jest to jedynie zabieg marketingowy lub sposób na to, by obniżyć koszty.
Wadą mieszanek jest także to, że utrudniają one rzetelną ocenę ilości czystego kwasu masłowego (każdy składnik ma inną zawartość procentową kwasu masłowego).
Dlatego oceniamy ilość czystego kwasu masłowego (maks 20 pkt) a nie samej soli. Podanie przez producenta ilości czystego kwasu masłowego, którą dostarcza suplement jest kryterium obecności w naszym rankingu ponieważ realna ilość czystego kwasu masłowego w suplemencie nie zawsze odpowiada jego zawartości wynikającej ze składu procentowego soli. Często jego ilość jest dużo niższa. Sól może być zanieczyszczona dodatkami czy wypełniaczami [1-9].
Na poniższej grafice znajdziesz punktację dla poszczególnych form chemicznych maślanu, ich ilości oraz ilości czystego kwasu masłowego:

Właściwości poszczególnych soli kwasu masłowego [Rozwiń]:
- Maślan sodu (Sodium Butyrate, NaB) jest najlepiej przebadaną solą kwasu masłowego pod kątem działania przeciwzapalnego, regeneracji nabłonka jelitowego, redukcji IBS-D (zespołu jelita drażliwego z dominującą biegunką), poprawy metabolizmu oraz wspierania bariery jelitowej. W badaniach klinicznych to właśnie maślan sodu dominuje jako substancja, którą przyjmują ludzie. Zawiera ok. 80% czystego kwasu masłowego. Oznacza to, że suplement, który zawiera 600 mg maślanu sodu, dostarcza realnie ok. 480 mg czystego kwasu masłowego. Maślan sodu jest formą stabilną, łatwą do mikrokapsułkowania oraz odpowiednią do wytwarzania w kapsułkach o przedłużonym uwalnianiu (DR)./
- Maślan potasu (Potassium Butyrate, KB) jest bardzo dobrą, fizjologiczną formą, ale rzadziej stosowaną. Maślan potasu jest równie skuteczny jak maślan sodu, a jon potasu jest naturalny dla środowiska jelitowego. W badaniach na modelach zwierzęcych i komórkowych działa przeciwzapalnie, wzmacnia barierę jelitową i wspiera metabolizm, choć badań klinicznych u ludzi jest mniej. Zawiera ok. 70% czystego kwasu masłowego. Oznacza to, że suplement, który zawiera 600 mg maślanu potasu, dostarcza realnie ok. 420 mg czystego kwasu masłowego. Przez część osób maślan potasu jest lepiej tolerowany niż maślan sodu, ma od niego bardziej neutralny profil jonowy, ale technologicznie jest trudniejszy do stabilizacji.
- Maślan wapnia (Calcium Butyrate, CaB) jest stabilny, ale zawiera najmniej czystego kwasu masłowego i ma gorszą rozpuszczalność. Maślan wapnia jest tańszy i stabilniejszy, ale ma najmniejszą biodostępność ze wszystkich soli kwasu masłowego. W środowisku jelitowym uwalnia kwas masłowy wolniej, ale często jest stosowany w przemyśle paszowym, bardziej niż w suplementach dla ludzi. Zawiera ok. 82% czystego kwasu masłowego. Oznacza to, że suplement, który zawiera 600 mg maślanu wapnia, dostarcza realnie 490 mg czystego kwasu masłowego. Maślan wapnia ma mniej badań klinicznych, a jego działanie zależy w znacznej mierze od technologii uwalniania (mikrokapsułki lub powłoki DR są niemal konieczne, aby dotarł do jelita grubego) [1-9].
Postać i technologia uwalniania (maks. 30 pkt)
W przypadku maślanu sodu kluczowe jest nie tylko to, ile go przyjmujemy, ale gdzie i w jaki sposób zostanie uwolniony. Substancja ta jest wrażliwa na kwaśne środowisko żołądka i szybko metabolizowana w górnych odcinkach jelita. Dlatego skuteczny preparat musi dotrzeć aż do jelita grubego [1], [8], [10-18].
Badania pokazują, że zwykłe, niepowlekane kapsułki uwalniają większość maślanu już w żołądku, co ogranicza jego działanie miejscowe. Formy dojelitowe i powlekane np. DRcaps®, enteric coating czy systemy pH-controlled release uwalniają maślan dopiero w okolicy krętniczo-kątniczej, co znacząco zwiększa ich efektywność.
Powłoka dojelitowa przesuwa uwalnianie maślanu o 2-3 godziny, dzięki czemu trafia on do jelita grubego.
Równie istotna jest technologia mikrokapsułkowania i przedłużonego uwalniania. Badania kliniczne z mikrokapsułkowanym maślanem (np. u pacjentów z IBD oraz IBS – zespół jelita drażliwego) pokazują, że taka postać skuteczniej modyfikuje mikrobiotę, zmniejsza stan zapalny i redukuje objawy żołądkowo-jelitowe [1], [8], [10-18].
To właśnie dlatego postać technologiczna ma w naszej ocenie tak dużą wagę. Dwóch suplementów z tą samą ilością maślanu nie można traktować jako równoważnych, jeśli jeden uwalnia się w żołądku, a drugi w jelicie grubym.
Uważamy, że forma dojelitowa (enteric) i mikrokapsułkowanie to nie „dodatki marketingowe”, lecz technologie, które realnie poprawiają efekty i komfort suplementacji.
Poniższa grafika pokazuje, jak oceniamy postać i technologię uwalniania maślanu [1], [8], [10-18].
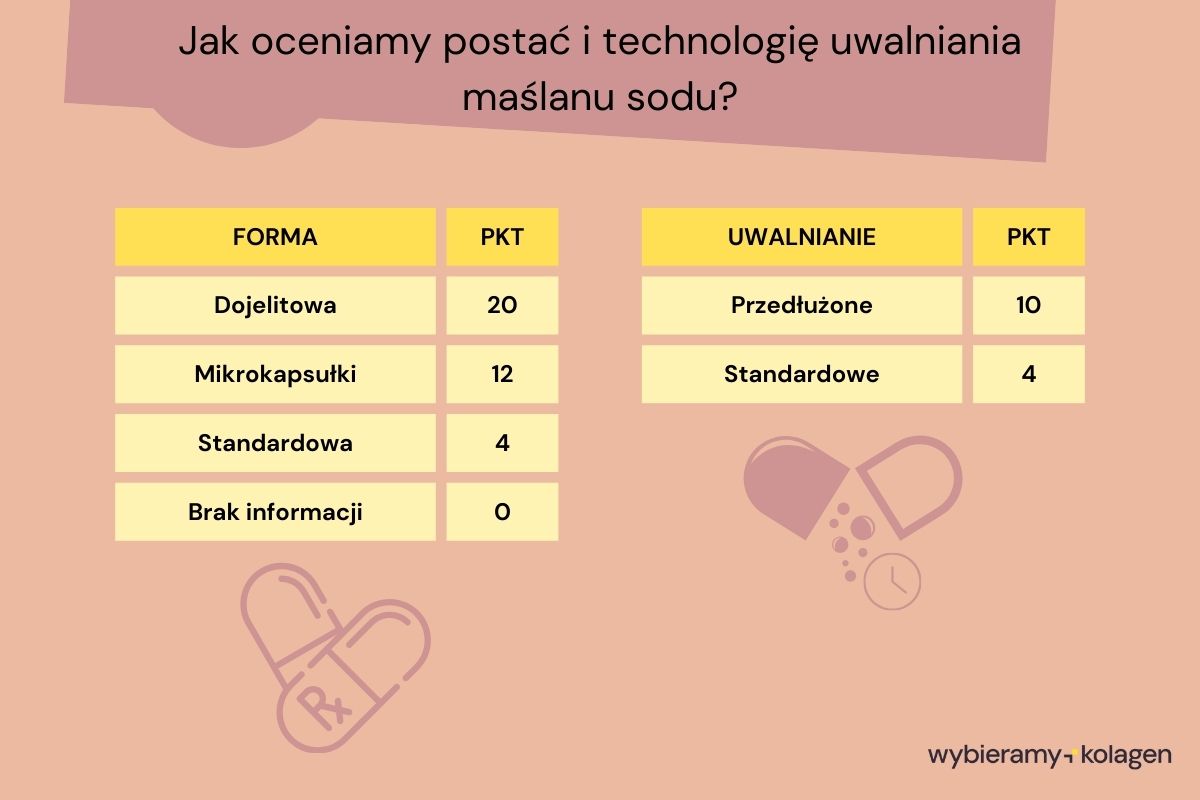
Dlaczego postać i technologia są tak ważne w przypadku maślanu sodu i innych maślanów? [Rozwiń]:
Kwas masłowy ma dwie naturalne cechy, które sprawiają, że technologia, w jakiej został podany, ma ogromne znaczenie:
- Maślan działa głównie w jelicie – szczególnie grubym. To właśnie tam kwas masłowy odżywia enterocyty, wzmacnia barierę jelitową, zmniejsza stan zapalny i wpływa na mikrobiotę. Zwykła kapsułka lub proszek uwalniają się zbyt wcześnie – najczęściej już w żołądku lub w górnym jelicie cienkim. Badania profilu uwalniania pokazują, że klasyczne formy maślanu niemal w całości uwalniają się w „fazie żołądkowej”, co oznacza, że tylko niewielka część dociera dalej – tam, gdzie faktycznie ma działać. Dlatego tak istotne są formy dojelitowe, które przechodzą przez żołądek nienaruszone i uwalniają maślan dopiero przy wyższym pH w jelitach [1], [8], [10-18].
- Maślan ma bardzo silny, nieprzyjemny zapach i smak – czysty maślan i jego sole pachną intensywnie „serowo-kiszonkowo”, czasem wręcz „fekalnie”. To naturalna właściwość krótkołańcuchowych kwasów tłuszczowych, ale sprawia ona, że suplement w postaci proszku lub zwykłej kapsułki może być trudny do przyjmowania. Rozwiązaniem jest mikrokapsułkowanie, czyli technologia, która zamyka maślan w małych cząstkach tłuszczowych lub polisacharydowych. Dzięki temu zapach jest praktycznie niewyczuwalny, kapsułki są znacznie łatwiejsze do przełknięcia, a dodatkowo można uzyskać kontrolowane, wolniejsze uwalnianie [1], [8], [10-18].
Dodatki (maks. 25 pkt)
W suplementach diety z maślanem skład „dodatkowy” ma znaczenie. To, czy produkt zawiera probiotyki, prebiotyki czy składniki metaboliczne, realnie wpływa na jego działanie. Dlatego w naszym systemie to osobna, ważna kategoria oceny — nie traktujemy maślanu jako izolowanej substancji, ale jako element ekosystemu jelit [19-28].
Najwyżej oceniamy dodatki, które wymieniamy niżej.
- Probiotyki – mikrobiota produkuje maślan naturalnie. Kwas masłowy nie jest tylko substancją, którą można dostarczyć z zewnątrz. W zdrowym jelicie jest wytwarzają go bakterie – głównie z grup Butyricicoccus, Faecalibacterium prausnitzii, Roseburia czy Eubacterium. Jeśli Twoja mikrobiota jest zubożona, ponieważ chorujesz na IBS, masz dysbiozę, stosujesz antybiotyki lub doświadczasz przewlekłego stresu, naturalna produkcja maślanu spada nawet o 50–70%. Z tego powodu dodatek probiotyków w suplementach z maślanem nie jest przypadkiem – to próba odtworzenia naturalnej fabryki maślanu w jelicie [19-22].
- Prebiotyki – bez „paliwa” probiotyki nie działają. Prebiotyki to składniki, które służą bakteriom jako pożywka i zwiększają produkcję maślanu w jelicie grubym. Suplementacja maślanu działa najlepiej, gdy równolegle wspiera się całą mikrobiotę jelit. Prebiotyk zwiększa liczebność Bifidobacterium, co w połączeniu z maślanem daje efekt synergii – większą odporność bariery jelitowej i bardziej stabilny mikrobiom [19-22].
- Witamina D3 – oba składniki działają w tych samych szlakach, które regulują odporność i zdrowie jelit. Badania pokazują, że maślan zwiększa ekspresję receptora witaminy D (VDR) oraz enzymów, które aktywują witaminę D. Dzięki temu wzmacnia działanie przeciwzapalne i barierowe w jelicie. W modelach zapalenia jelit wykazano, że maślan i witamina D razem działają silniej niż każdy składnik osobno, co sugeruje prawdziwą synergię biologiczną [23-26].
- Dodatki metaboliczne – mogą wzmacniać to, jak działa maślan sodu. Niektóre suplementy zawierają również składniki, które nie są obowiązkowe, ale mogą wspierać działanie metaboliczne lub energetyczne maślanu. Na przykład L-karnityna wspiera transport kwasów tłuszczowych do mitochondriów, a maślan jest jednym z kluczowych paliw energetycznych dla enterocytów. Z kolei witamina D zwiększa integralność bariery jelitowej i działa przeciwzapalnie, przez co efekt synergii z maślanem jest biologicznie uzasadniony. Nie są to składniki „must have”, ale uwzględniamy je w naszej ocenie jakości suplementu [27-28].
Poniższe grafiki pokazują, jak oceniamy dodatki do suplementów z maślanem [19-28].


Czysty skład (maks. 15 pkt)
Od kilku lat widać wyraźny trend na rynku splementów – dodatki, które wcześniej były „standardowe”, dziś są wycofywane lub ograniczane. Najlepszym tego przykładem jest dwutlenek tytanu (E171), którego Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA) od 2021 r. nie uznaje już za bezpieczny dodatek do żywności, głównie z powodu obaw o genotoksyczność i kumulację cząstek w organizmie. To, co jeszcze kilka lat temu uchodziło za „normalny” składnik kapsułki, dziś już nie spełnia aktualnych standardów bezpieczeństwa [29-31].
Gdy oceniamy suplementy z maślanem sodu, czysty skład nie jest „estetycznym dodatkiem”, tylko realnym kryterium jakości i bezpieczeństwa.
W kategorii "Czysty skład" każdy suplement diety z maślanem otrzymuje od nas na start 15 pkt – jeśli ma czysty skład, zachowuje je. Nasz algorytm przyznaje punkty ujemne za zbędne składniki dodatkowe, według podziału:
- dodatki GRUPA I – dodatki technologiczne, bezpieczne -0 pkt (za każdy),
- dodatki GRUPA II – dodatki bezpieczne, ale niekonieczne – olej palmowy, słodziki i aromaty -1 pkt (za każdy),
- dodatki GRUPA III – dodatki słabo akceptowalne, sztuczne barwniki, konserwanty, tłuszcze trans -3 pkt (za każdy).
Maślan sodu to suplement diety, który przyjmujemy długoterminowo – przy IBS, SIBO, przewlekłych dolegliwościach jelitowych, po antybiotykoterapii czy w profilaktyce. Oznacza to, że:
- suplement stosujemy codziennie, często przez wiele miesięcy,
- nawet „małe” dodatki, jeśli są zbędne lub kontrowersyjne, kumulują się przy takim stosowaniu,
- osoby, które sięgają po maślan sodu, to często pacjenci wrażliwi (IBS, biegunki, stany zapalne, alergie), u których każdy dodatkowy barwnik czy tłuszcz trans może nasilać objawy.
Dlatego uważamy, że suplement jelitowy powinien być możliwie „czysty” – mieć tyle dodatków, ile trzeba z punktu widzenia technologii – i ani grama więcej [29-32].

Dlaczego czysty skład jest tak ważny w przypadku maślanu? [Rozwiń]:
W części maślanów nośnikiem są uwodornione lub częściowo uwodornione (utwardzone) tłuszcze (np. olej palmowy), które zwiększają udział tłuszczów nasyconych w Twojej diecie. Zarówno źródła naukowe, jak i instytucje zdrowia publicznego podkreślają, że nadmiar tłuszczów nasyconych zwiększa stężenie LDL („złego cholesterolu”) i ryzyko sercowo-naczyniowe. W dokumentach Komisja Europejska jasno wskazuje, że przy reformulacji żywności należy unikać zastępowania tłuszczów trans dużymi ilościami tłuszczów nasyconych [29-32].
Z tego powodu suplement, który ma wspierać zdrowie jelit, nie powinien jednocześnie dorzucać zbędnych porcji „twardych” tłuszczów. Dodatki typu uwodornione tłuszcze czy duże ilości oleju palmowego obniżają naszą ocenę „czystego składu”.
Transparentność i zaufanie – trend „clean label”. Coraz więcej badań konsumenckich pokazuje, że ludzie świadomie szukają produktów z krótką listą składników, bez sztucznych dodatków i z prostym, przejrzystym składem.
Źródła [Rozwiń]:
- La Monica, Michael & Kirby, Trevor & Hartshorn, Shelley & Gustat, Ashley & Grdic, Jodi & Sandrock, Jennifer. (2025). A Pharmacokinetic Comparison of Three Butyrate Products: Original Research. Journal of Exercise and Nutrition. 8. 10.53520/jen2025.103189.
- Yağcılar, A. P., Çağlar, E. Ş., & Üstündağ Okur, N. (2025). Analytical Method Development and Validation: Calcium Butyrate. Analytica, 6(4), 42. https://doi.org/10.3390/analytica6040042.
- Głąbień, M., Miłkowski, P., Kuśnierz, A., Kusiak, K., Aleksandrowicz, D., Wieczorek, O., … Kondratowicz, A. (2024). Sodium Butyrate as Gut Microbiota Modulators: Mechanisms of Action and Potential Clinical Applications - Literature Review and New Perspectives. Quality in Sport, 27, 55233. https://doi.org/10.12775/QS.2024.27.55233.
- Banasiewicz, T., Domagalska, D., Borycka-Kiciak, K., & Rydzewska, G. (2020). Determination of butyric acid dosage based on clinical and experimental studies - a literature review. Przeglad gastroenterologiczny, 15(2), 119–125. https://doi.org/10.5114/pg.2020.95556
- Mitrović, M., Stanković Popović, V., Erceg, S., Perišić Mitrović, M., Dobrosavljević, A., Stupar, A., Vuković, P., Zlatković, D., & Svorcan, P. (2025). Exploring the Potential of Oral Butyrate Supplementation in Metabolic Dysfunction-Associated Steatotic Liver Disease: Subgroup Insights from an Interventional Study. International Journal of Molecular Sciences, 26(12), 5561. https://doi.org/10.3390/ijms26125561.
- Liu, H., Wang, J., He, T., Becker, S., Zhang, G., Li, D., & Ma, X. (2018). Butyrate: A Double-Edged Sword for Health?. Advances in nutrition (Bethesda, Md.), 9(1), 21–29. https://doi.org/10.1093/advances/nmx009.
- Canani, R. B., Costanzo, M. D., Leone, L., Pedata, M., Meli, R., & Calignano, A. (2011). Potential beneficial effects of butyrate in intestinal and extraintestinal diseases. World journal of gastroenterology, 17(12), 1519–1528. https://doi.org/10.3748/wjg.v17.i12.1519.
- Russo, R., Santarcangelo, C., Badolati, N., Sommella, E., De Filippis, A., Dacrema, M., Campiglia, P., Stornaiuolo, M., & Daglia, M. (2021). In vivo bioavailability and in vitro toxicological evaluation of the new butyric acid releaser N-(1-carbamoyl-2-phenyl-ethyl) butyramide. Biomedicine & pharmacotherapy = Biomedecine & pharmacotherapie, 137, 111385. https://doi.org/10.1016/j.biopha.2021.111385.
- Gerunova LK, Gerunov TV, P’yanovaLydia G., Lavrenov AV, Sedanova AV, Delyagina MS, Fedorov YN, Kornienko NV, Kryuchek YO, Tarasenko AA. Butyric acid and prospects for creation of new medicines based on its derivatives: a literature review. J Vet Sci. 2024 Mar;25(2):e23. https://doi.org/10.4142/jvs.23230
- Roda, A., Simoni, P., Magliulo, M., Nanni, P., Baraldini, M., Roda, G., & Roda, E. (2007). A new oral formulation for the release of sodium butyrate in the ileo-cecal region and colon. World journal of gastroenterology, 13(7), 1079–1084. https://doi.org/10.3748/wjg.v13.i7.1079.
- Caban, M., Pikus, E., Czarnecka-Chrebelska, K., Oszajca, K., Witusik-Perkowska, M., Dudek, J., Szemraj, J., Brzeziańska-Lasota, E., & Talar-Wojnarowska, R. (2025). Use of Sodium Butyrate and Its Microencapsulated Forms in Intestinal Diseases-Current Clinical Approach. Digestive diseases and sciences, 10.1007/s10620-025-09536-4. Advance online publication. https://doi.org/10.1007/s10620-025-09536-4
- Facchin, S., Vitulo, N., Calgaro, M., Buda, A., Romualdi, C., Pohl, D., Perini, B., Lorenzon, G., Marinelli, C., D'Incà, R., Sturniolo, G. C., & Savarino, E. V. (2020). Microbiota changes induced by microencapsulated sodium butyrate in patients with inflammatory bowel disease. Neurogastroenterology and motility, 32(10), e13914. https://doi.org/10.1111/nmo.13914
- Sadurní, M., Barroeta, A. C., Sol, C., Puyalto, M., & Castillejos, L. (2022). Short Communication: Evaluation of Intestinal Release of Butyric Acid from Sodium Butyrate Protected by Salts of Medium-Chain Fatty Acids in Broiler Chickens. Animals : an open access journal from MDPI, 12(24), 3525. https://doi.org/10.3390/ani12243525.
- Onrust, L., Baeyen, S., Haesebrouck, F., Ducatelle, R., & Van Immerseel, F. (2020). Effect of in feed administration of different butyrate formulations on Salmonella Enteritidis colonization and cecal microbiota in broilers. Veterinary research, 51(1), 56. https://doi.org/10.1186/s13567-020-00780-2
- Augustin, Mary Ann & Abeywardena, M. & Head, R. & Lockett, Trevor & Luca, A. & Sanguansri, Luz. (2011). Effects of microencapsulation on the gastrointestinal transit and tissue distribution of a bioactive mixture of fish oil, tributyrin and resveratrol. Journal of Functional Foods. 3. 25-37. 10.1016/j.jff.2011.01.003.
- Li, Caiming & Li, Zexi & Liu, Tonghui & Gu, Zhengbiao & Ban, Xiaofeng & Tang, Xiaoshu & Yan, Hong & Cheng, Li & Li, Zhaofeng. (2021). Encapsulating tributyrin during enzymatic cyclodextrin synthesis improves the solubility and bioavailability of tributyrin. Food Hydrocolloids. 113. 106512. 10.1016/j.foodhyd.2020.106512.
- Krokowicz, L., Stojcev, Z., Kaczmarek, B. F., Kociemba, W., Kaczmarek, E., Walkowiak, J., Krokowicz, P., Drews, M., & Banasiewicz, T. (2014). Microencapsulated sodium butyrate administered to patients with diverticulosis decreases incidence of diverticulitis--a prospective randomized study. International journal of colorectal disease, 29(3), 387–393. https://doi.org/10.1007/s00384-013-1807-5.
- Lewandowski, K., Kaniewska, M., Karłowicz, K., Rosołowski, M., & Rydzewska, G. (2022). The effectiveness of microencapsulated sodium butyrate at reducing symptoms in patients with irritable bowel syndrome. Przeglad gastroenterologiczny, 17(1), 28–34. https://doi.org/10.5114/pg.2021.112681
- Swanson, K. S., Gibson, G. R., Hutkins, R., Reimer, R. A., Reid, G., Verbeke, K., Scott, K. P., Holscher, H. D., Azad, M. B., Delzenne, N. M., & Sanders, M. E. (2020). The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nature reviews. Gastroenterology & hepatology, 17(11), 687–701. https://doi.org/10.1038/s41575-020-0344-2
- Kolida, S., & Gibson, G. R. (2011). Synbiotics in health and disease. Annual review of food science and technology, 2, 373–393. https://doi.org/10.1146/annurev-food-022510-133739
- Markowiak, P., & Śliżewska, K. (2017). Effects of Probiotics, Prebiotics, and Synbiotics on Human Health. Nutrients, 9(9), 1021. https://doi.org/10.3390/nu9091021
- Rivière, A., Selak, M., Lantin, D., Leroy, F., & De Vuyst, L. (2016). Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut. Frontiers in microbiology, 7, 979. https://doi.org/10.3389/fmicb.2016.00979
- Huang, F.-C., & Huang, S.-C. (2024). Unveiling the Novel Benefits of Co-Administering Butyrate and Active Vitamin D3 in Mice Subjected to Chemotherapy-Induced Gut-Derived Pseudomonas aeruginosa Sepsis. Biomedicines, 12(5), 1026. https://doi.org/10.3390/biomedicines12051026.
- Gao, H., Zhao, X., Guo, Y., Li, Z., & Zhou, Z. (2024). Coated sodium butyrate and vitamin D3 supplementation improve gut health through influencing intestinal immunity, barrier, and microflora in early-stage broilers. Journal of the science of food and agriculture, 104(7), 4058–4069. https://doi.org/10.1002/jsfa.13288.
- Wu, S., Zhang, Y. G., Lu, R., Xia, Y., Zhou, D., Petrof, E. O., Claud, E. C., Chen, D., Chang, E. B., Carmeliet, G., & Sun, J. (2015). Intestinal epithelial vitamin D receptor deletion leads to defective autophagy in colitis. Gut, 64(7), 1082–1094. https://doi.org/10.1136/gutjnl-2014-307436.
- Ullah H. (2025). Gut-vitamin D interplay: key to mitigating immunosenescence and promoting healthy ageing. Immunity & ageing : I & A, 22(1), 20. https://doi.org/10.1186/s12979-025-00514-y.
- Babenkova, P., Gureev, A., Sadovnikova, I., Burakova, I., Smirnova, Y., Pogorelova, S., Morozova, P., Gribovskaya, V., Adzhemian, D., & Syromyatnikov, M. (2025). Changes in L-Carnitine Metabolism Affect the Gut Microbiome and Influence Sexual Behavior Through the Gut–Testis Axis. Microorganisms, 13(8), 1751. https://doi.org/10.3390/microorganisms13081751.
- Flegiel, E., Piotrowska, M., Ptasznik, M., Baran, A., Lenart, J., Podrażka, M., … Adamczyk, M. (2024). Review of the effects of sodium butyrate on obesity, inflammatory bowel disease, pregnancy and colorectal cancer. Prospects in Pharmaceutical Sciences, 22(4), 7–15. https://doi.org/10.56782/pps.229.
- EFSA FAF Panel. (2021). Safety assessment of titanium dioxide (E171) as a food additive. EFSA Journal, 19(5), 6585. https://doi.org/10.2903/j.efsa.2021.6585.
- https://www.efsa.europa.eu/pl
- Statham, B. (2014). E213. Tabele dodatków i składników chemicznych (K. Tryc, Trans.). Wydawnictwo RM. (Original work published 2006 as The Chemical Maze – Shopping Companion.
- Grant, Kara & Gallardo, Karina & Mccluskey, Jill. (2021). Consumer preferences for foods with clean labels and new food technologies. Agribusiness. 37. 764-781. 10.1002/agr.21705.
- Dutheil F, Oueslati T, Delamarre L, Castanon J, Maurin C, hiambaretta F, Baker JS, Ugbolue UC, Zak M, Lakbar I, Pereira B, Navel V. Myopia and Near Work: A Systematic Review and Meta-Analysis. Int J Environ Res Public Health. 2023 Jan 3;20(1):875. doi: 10.3390/ijerph20010875. PMID: 36613196; PMCID: PMC9820324.
- Amiri, P., Hosseini, S. A., Roshanravan, N., Saghafi-Asl, M., & Tootoonchian, M. (2023). The effects of sodium butyrate supplementation on the expression levels of PGC-1α, PPARα, and UCP-1 genes, serum level of GLP-1, metabolic parameters, and anthropometric indices in obese individuals on weight loss diet: a study protocol for a triple-blind, randomized, placebo-controlled clinical trial. Trials, 24(1), 489. https://doi.org/10.1186/s13063-022-06891-9
- Coppola, S., Nocerino, R., Paparo, L., Bedogni, G., Calignano, A., Di Scala, C., de Giovanni di Santa Severina, A. F., De Filippis, F., Ercolini, D., & Berni Canani, R. (2022). Therapeutic Effects of Butyrate on Pediatric Obesity: A Randomized Clinical Trial. JAMA network open, 5(12), e2244912. https://doi.org/10.1001/jamanetworkopen.2022.44912
- Pituch, A., Walkowiak, J., & Banaszkiewicz, A. (2013). Butyric acid in functional constipation. Gastroenterology Review/Przegląd Gastroenterologiczny, 8(5), 295-298. https://doi.org/10.5114/pg.2013.38731.
 Jak oceniamy suplementy z maślanem sodu?
Jak oceniamy suplementy z maślanem sodu?






